Oxeiptose – ein Zelltod-Signalweg, der durch reaktive Sauerstoffradikale (reactive oxygen species) induziert wird und vor pathologischen Entzündungen schützt
Forschungsbericht (importiert) 2017 - Max-Planck-Institut für Biochemie
Leben oder sterben lassen – kritische Entscheidungsfindungen in Zellen
Zu leben oder zu sterben gehört zu den fundamentalsten Entscheidungen, die eine Zelle treffen kann. Es gibt eine Reihe von gut studierten Signalwegen, welche exogene und intrazelluläre Signale erkennen und, falls nötig, die Zelle in den programmierten Zelltod führen. Je nach Signalweg sind die Konsequenzen für die Zelle und den Organismus unterschiedlich. Zelltod durch Nekroptose, zum Beispiel, bewirkt die Ruptur der Zellmembran und das Freisetzen von intrazellulärem Inhalt, der das Immunsystem aktiviert. Im Gegensatz dazu werden im Zuge von Apoptose Membran-Abschnürungen gebildet, die Zelle wird pyknotisch und bildet sich zurück. Das Immunsystem wird in diesem Fall nicht aktiviert. In den letzten Jahren wurden die dem Zelltod unterliegenden Signalwege und auch die Relevanz des programmierten Zelltodes bei diversen Erkrankungen detailliert untersucht. Mutationen in Proteinen, die in Zelltod Signalwege involviert sind, sind oft assoziiert mit Krebs, Entwicklungsstörungen und Infektionserkrankungen.
Verschiedene Signale können zu Zelltod führen und die unterschiedlichen pro- und antiinflammatorischen Signalwege bedienen. Zu den bekannten Auslösern des programmierten Zelltodes gehören unter anderem reaktive Sauerstoffradikale (reactive oxygen species, ROS), die im Zuge physiologischer und pathologischer Vorgänge in der Zelle gebildet werden. Obwohl die Relevanz von ROS bekannt ist, ist nicht klar, welche Proteine toxische Mengen an ROS erkennen und wie eine solche Erkennung zur Aktivierung von Zelltod-Signalwegen führt.
Oxeiptose – ein neuer Zelltod-Signalweg, der Sauerstoffradikale erkennt
Mithilfe einer Kombination von massenspektrometrischen Untersuchungen und Funktionsanalysen in vitro und in vivo konnte ein neuer Signalweg entschlüsselt werden, über den toxische Mengen an ROS erkannt werden können und der zum Tod der Zelle führt. Da es sich hierbei um einen neuen, bisher unbekannten Signalweg handelt, nennen wir diesen Signalweg Oxeiptose – Tod, hervorgerufen durch Sauerstoffradikale (Abb. 1; [1]).
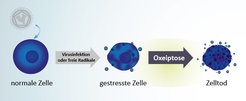
Das zelluläre Protein KEAP1 fungiert als ROS Sensor und ist für seine zytoprotektive Rolle bekannt. Durch Oxidation von C-terminalen Cysteinen ändert KEAP1 seine Struktur und bewirkt so die Aktivierung eines Transkriptionsfaktors, der für die Expression von Proteinen verantwortlich ist, die intrazelluläre ROS neutralisieren können. Durch diesen Mechanismus wird die Menge an intrazellulärem ROS reguliert. Erstaunlicherweise ändert KEAP1 nach Stimulation durch große Mengen an ROS seine Funktion und konvertiert zu einem Zelltod-Vermittler. In diesem Modus aktiviert das Protein eine mitochondriale Phosphatase, PGAM5, die wiederum das Effektorprotein AIFM1 an einem evolutionär hochkonservierten Serin dephosphoryliert. Die Dephosphorylierung von AIFM1 ist ausreichend, um den Zelltod zu initiieren. Experimentelle Depletion von Komponenten dieses Signalweges erhöht die Toleranz von Zellen für hohe Mengen an ROS.
Essentielle Rolle von Oxeiptose bei viralen Infektionen
Oxeiptose wird auch im Zuge von viralen Infektionen aktiviert; das Ausschalten von Komponenten des Oxeiptose Signalweges wiederum verhindert in Zellkulturexperimenten Virus-induzierten Zelltod. Die Signifikanz dieses Zelltodmechanismus wird dadurch unterstrichen, dass evolutionär unterschiedliche Viren Proteine kodieren, die diesen Signalweg aktiv modulieren können. Oxeiptose spielt auch in vivo eine bedeutsame Rolle: Mäuse, die hohen Konzentrationen von ROS-induzierendem Ozon ausgesetzt sind, zeigen Entzündungsprozesse in der Lunge. Wenn in diesen Tieren PGAM5, ein essentieller Teil des Oxeiptose Signalweges, mutiert vorliegt, sind die Ozon-induzierten Entzündungsprozesse signifikant aggressiver. Entzündungsmarker wie Zytokine und Proteine, die durch Gewebeschädigung freigesetzt werden, sind erhöht und das respiratorische Epithel wird stark in Mitleidenschaft gezogen. Ähnliche Veränderungen sieht man bei Infektionen mit Influenzavirus. Auch in diesem Fall zeigen PGAM5 knockout Tiere eine starke Lungenentzündung und schwere Gewebeschäden, die zu einem schwerwiegenden Krankheitsbild führen. Bei Oxeiptose handelt es sich demzufolge um einen Zelltod, der anti-inflammatorisch aktiv ist. Können Zellen durch Mutationen in kritischen Komponenten diesem Zelltod nicht eingehen, nimmt ein inflammatorischer Zelltod Programm überhand und bewirkt so schwerwiegende Gewebeschäden.
Wir vermuten, dass Oxeiptose in vielen pathologischen Reaktionen eine Rolle spielt. Erhöhte ROS Konzentrationen sind zum Beispiel assoziiert mit allergischen Reaktionen, Autoimmunkrankheiten, Krebs und Infektionen mit Erregern. Mutationen in Proteinen, die im Oxeiptose Signalweg eine Rolle spielen, wurden unter anderem in Lungen und Gallenblasenkrebs identifiziert, und manche Krebsarten zeigen eine reduzierte Expression dieser Signalproteine.
Durch die Entdeckung dieses Signalweges erhalten wir Einblicke in Abläufe, die im Zuge pathologischer Situationen stattfinden und legen so eine Grundlage für therapeutische Ansätze, die es möglich machen, den regulierten Zelltod sowie das Entzündungsgeschehen in pathologischen Situationen zu regulieren.
